Methanhydrate

Methanhydrate sind eine häufige Form von Gashydraten. Diese gelten als möglicher Ersatz für Kohle, Öl und Erdgas. Sie bilden sich vor allem in Permafrostregionen und im Meer an Kontinentalrändern.
Wasser und Gas bilden bei hohem Druck und niedrigen Temperaturen die feste Verbindung: Gashydrat. Bereits 1810 gelang es dem britischen Naturforscher Sir Humphrey Davy eher zufällig, eine derartige eisähnliche Substanz (Chlorhydrat) herzustellen, indem er Chlorgas unter Druck durch Wasser perlen ließ. Für mehr als ein Jahrhundert galten Gashydrate jedoch als chemische Kuriosität und wurden kaum beachtet. In den dreißiger Jahren des 20. Jahrhunderts wurden sie in der Öl- und Gasindustrie bekannt, als sich herausstellte, dass unbeabsichtigte Gashydratbildung für Transportprobleme in Pipelines verantwortlich war. Es bildete sich bei herabgesetzten Temperaturen festes Gashydrat aus unter Druck stehendem Gas (vorwiegend Methan) und verstopfte die Leitungssysteme.
In der Natur kommen Hydrate verschiedener Gase vor, wie beispielsweise Stickstoff-Hydrate im Eisschild Grönlands oder auf anderen Planeten Kohlendioxid-Hydrate. Häufig sind Methanhydrate, die aufgrund ihrer physikalischen Stabilitätsbedingungen prinzipiell in Meeressedimenten sowie in Permafrostböden der polaren Regionen vorkommen.
Was sind Gashydrate?
Gashydrate sind nicht-stöchiometrische Verbindungen, wobei die Wassermoleküle Käfigstrukturen aufbauen , in denen Gasmoleküle eingeschlossen sind. Sie werden deshalb auch Einschlussverbindungen oder Clathrate (lat.: clatratus = Käfig) genannt. Generell können Gashydrate bei ihrer Bildung gleichzeitig verschiedene Gasmoleküle, abhängig von ihrer Häufigkeit in der Umgebung, in getrennten Käfigen einbauen. Neben CH4 sind es in der Natur vor allem H2S, CO2 und seltener höhere Kohlenwasserstoffe.
Zur Bildung von Gashydrat sind neben der Verfügbarkeit einer ausreichenden Menge von Gas und Wasser die Druck-Temperatur-Bedingungen die entscheidenden Faktoren. Gashydrate sind nur bei hohen Drücken und relativ niedrigen Temperaturen stabil, wobei die Anwesenheit von H2S, CO2 und höheren Kohlenwasserstoffen die Hydrat-Gas-Phasengrenze zu höheren Temperaturen verschiebt. Stickstoff-Gas und im Wasser gelöste Salze verschieben die Phasengrenze dagegen zu niedrigeren Temperaturen.
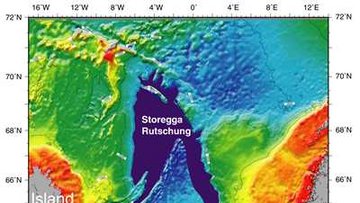
Während die physikalischen Parameter Druck und Temperatur die generell mögliche Verteilung der Methanhydrate beschreibt, ist ein limitierender Faktor die allgemeine Verfügbarkeit einer ausreichenden Menge von Gas, vornehmlich CH4. Im Ozean stammt das Methan zu einem großen Anteil aus dem fermentativen Abbau organischer Komponenten bzw. aus der bakteriellen CO2-Reduktion in den Ablagerungen. Teilweise wird es aber auch durch thermokatalytische Umwandlungsprozesse in tieferen Sedimenten gebildet. Die bei weitem höchsten Anteile an CH4 werden im Bereich der Kontinentalränder gebildet, wo durch hohe Planktonproduktivität der Ozeane und durch hohe Sedimentationsraten große Mengen von organischem Material im Sediment für die Gasbildung zur Verfügung gestellt werden. Daher sind Gashydrate an fast allen passiven und aktiven Kontintalrändern zu finden, aber auch im Kaspischen Meer, im Schwarzen Meer, im Mittelmeer und im Baikalsee.
Quelle: https://www.weltderphysik.de/gebiet/technik/energie/fossile-quellen/methanhydrate/